국내 연구진, 유년기 약물 치료 통한 자폐 완치 가능성 동물실험으로 증명

▲ 자폐 스펙트럼 장애는 언어, 의사소통 발달 등이 지연된 발달 장애를 뜻한다. 스펙트럼 장애라는 명칭이 내포하는 것처럼 같은 질환을 가져다 사람마다 나타나는 증상이 다르다. ⓒFlickr
자폐 증상 완화를 위해서는 3세 이하 영유아 시절에 보이는 변화에 더 주목해야 할 것으로 보인다. 기초과학연구원(IBS)이 이끄는 국내 공동연구진은 동물실험 결과를 토대로 유년기 자폐를 조기 진단하고, 집중적인 약물치료를 통해 자폐 증상을 평생 완화시킬 수 있다는 가능성을 제시했다. 실험에 쓰인 자폐 모델 생쥐는 아직 어미의 젖을 떼지 않은 3주령. 사람으로 치면 3세 이하의 유년기에 해당된다.
자폐 증상, 청소년기에 주춤하다 성인 때 재발
자폐증(자폐 스펙트럼 장애)은 세계 인구의 약 2% 정도에서 발병하는 뇌 발달장애의 한 종류다. 사회적 상호작용 결여, 반복 행동 등이 대표 증상이지만 병인이나 치료법에 대해서는 아직 완벽히 밝혀지지 않았다. 자폐를 유발하는 뇌 변화는 주로 유년기에 시작되지만, 유년기 뇌의 변화가 성인이 될 때까지 지속적으로 영향을 주는지 여부도 불분명했다.
IBS 뇌과학 이미징 연구단은 자폐 모델 생쥐의 자폐 증상이 성장 과정에 따라 어떻게 달라지는지 분석했다. 자폐 유발 유전자 중 하나인 ‘MYT1L 유전자’를 제거한 실험쥐는 사회성이 저하되고 반복행동이 증가하는 등 자폐 증상이 나타났다. 본래 쥐를 뒤집어 놓으면 다시 자세를 똑바로 바로잡는 ‘뒤집기 반사’ 행동을 하는데, 자폐 유발 생쥐의 뒤집기 반사 행동은 매우 빨라졌다. 또, 다른 생쥐 혹은 장난감과 함께 보내는 시간이 유사했다. 사회성이 떨어졌다는 의미다. 계속 뜀박질을 반복하거나, 구멍에 코를 들이미는 기이한 행동도 반복했다.
흥미로운 점은 MYT1L 결손 생쥐의 자폐 증상은 청소년기에는 나타나지 않다가 성체 시기에 다시 강하게 나타났다는 점이다. 연구진은 전사체(생산된 모든 RNA 분자의 합) 분석을 통해 성장 과정에 따라 자폐 발생 메커니즘을 분석했다. MYT1L이 결손된 유년기 생쥐는 뇌의 전전두엽에서 ‘흥분성 시냅스’의 수와 신호전달이 눈에 띄게 감소했다. 시냅스는 흥분성 시냅스와 억제성 시냅스로 구분되는데, 두 시냅스 간 균형이 깨지면 뇌 정신질환이 유발된다. 이와 달리 성체기 MYT1L 결손 생쥐의 뇌에서는 억제성 시냅수와 신호전달이 증가했다. MYT1L 유전자에 생긴 이상이 유년기에 뇌 변화를 일으키기 시작하고, 오랜 기간 축적되어 있다가 성체기에는 다른 메커니즘으로 자폐 증상을 유발한다는 의미다.
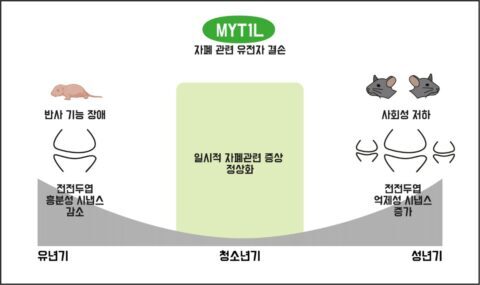
▲ 자폐 유발 유전자 중 하나인 ‘MYT1L’이 결손된 유년기 생쥐는 뇌 전전두엽에서 흥분성 시냅스가 감소하며 반사 기능 장애 등을 보인다. 이 생쥐의 자폐 증상은 청소년기에는 나타나지 않지만, 성년기가 되면 억제성 시냅스가 증가하며 사회성 저하, 반복 행동 등의 형태로 나타난다. ⓒIBS
이번 연구의 공동 제1저자인 김효성 KAIST 석박통합과정 연구원은 “유년기에 발생한 유전자 결핍이 청소년기에는 눈에 띄지 않다가 성체기에 본격적으로 증상을 나타낸다”며 “증상 완화 및 치료를 위해서는 유년기 조기 진단이 중요하다는 의미”라고 설명했다. 연구결과는 9월 21일 국제학술지 ‘셀 리포츠(Cell Reports)’에 실렸다.
젖먹이 생쥐에게 모유 통해 약물 전달, 평생에 걸친 치료 효과
이어 연구진은 또 다른 자폐 모델 생쥐를 이용해 조기 치료를 통한 완치 가능성도 확인했다. 이 연구에서 연구진은 또 다른 자폐 유발 유전자 중 하나인 ‘ARID1B’를 결손시킨 모델 쥐를 이용했다. ARID1B가 결손된 유년기 쥐는 어미로부터 분리되었을 때 어미를 찾기 위해 초음파로 울음소리를 내는 능력이 떨어졌다.
연구진은 자폐 유발 유전자 중 하나인 ‘ARID1B 단백질’이 결여된 쥐는 사회성 저하 및 반복 행동을 보임을 확인했다. 또 성체기에는 정상 쥐에 비해 처음 보는 생쥐와의 사회적 교류를 하지 않았고, 털을 다듬는 그루밍 행동 등을 반복적으로 보였다. ARID1B 돌연변이 생쥐의 유전자를 분석한 결과, 유년기 시절 ARID1B 결손이 뇌 전전두엽의 흥분성 시냅스 수를 감소시키는 것으로 확인됐다. 이는 청소년기와 성체 시기 생쥐의 흥분성 시냅스 기능 감소로 이어졌다.
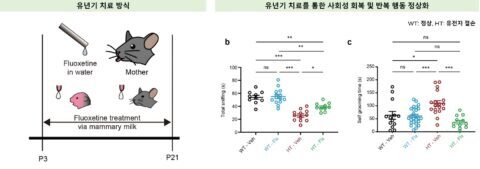
▲ 연구진은 자폐를 모유 수유를 통해 유발시킨 새끼 쥐에게 약물을 전달했다(왼쪽). 유년기에 3주 정도 집중적인 약물 치료를 받은 쥐는 성체가 되어서도 사회성과 반복행동이 정상 생쥐와 유사한 것으로 나타났다. ⓒIBS
뇌의 변화가 유년기에 시작된다는 점에 착안, 연구진은 실험쥐에게 흥분성 시냅스를 항진시키는 약물인 ‘플루옥세틴(Fluoxetine)’을 생후 3주 동안 투여했다. 연구진은 어미 쥐에게 풀루옥세틴을 희석한 약물을 주입하고, 모유 수유를 통해 새끼 쥐에게 간접적으로 전달했다. 약물치료를 받은 돌연변이 생쥐는 정상 생쥐와 유사한 수준의 사회성과 반복 행동을 보였다. 시냅스의 신호 전달과 수 역시 정상화됐다. 이후 치료를 중단해도 그 효과가 성체기까지 이어졌다.
연구결과는 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’ 8월 27일자에 실렸다.
가정에서의 관찰 및 행동치료가 자폐 아동 증상 완화에 도움
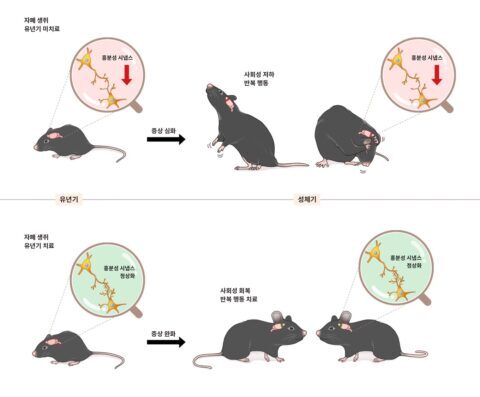
▲ 흥분성 시냅스의 수와 기능에 이상이 생기면 자폐 증상이 유발된다. IBS 연구진은 유년기 집중적 약물치료로 사회성 저하, 반복 행동 등 자폐 증상을 성체기까지도 완화됨을 동물실험으로 확인했다. ⓒIBS
물론 이번 연구는 동물 실험 수준에서 진행된 것이기 때문에 치료 효과를 사람에게서 확인할 때까지는 긴 시간이 걸릴 것으로 보인다. 게다가 오늘 날 규명된 자폐 유발 유전자는 1,000여 개다. 일련의 연구는 아직 소수의 유전자를 바탕으로 진행된 만큼, 수많은 후속연구가 진행돼야 인간 자폐 치료의 가능성까지 확인할 수 있을 것으로 보인다. 다만, 유년기 치료 약물치료가 성년기까지 오랫동안 지속되는 치료효과(long-lasting effect)를 보임을 최초로 확인한 연구인만큼, 여러 후속 연구를 견인하여 자폐 완치에 한 걸음 더 다가가는 계기가 될 것으로 보인다.
연구를 이끈 김은준 IBS 시냅스 뇌질환 연구단장은 “여러 연구를 통해 아이를 사랑으로 대하고, 즐거운 상황에 놓이도록 하는 ‘행동 치료’가 자폐 증상 완화에 도움이 된다는 것이 확인됐다”며 “자폐 증상을 완화할 가능성이 있는 ‘골든타임’ 동안 부모가 희망을 잃지 않고 아이들에게 많은 관심을 쏟아주길 바라본다”고 덧붙였다.
자폐 치료의 ‘골든타임’ 찾았다 – Sciencetimes
www.sciencetimes.co.kr
'시사교육배움 > 아기는' 카테고리의 다른 글
| 표선·성산 7개 초등학교 대상 IB 학교 설명회 열려 (0) | 2022.12.20 |
|---|---|
| 강릉 사는 4인 가족인데요, '핫플'은 못 가겠습니다 (0) | 2022.09.29 |
| 오은영 박사의 부모 10계명 (0) | 2022.04.08 |
| 아이의 인지적, 정서적 발달을 결정짓는 3가지 마법의 열쇠 (0) | 2021.10.26 |
| 부모가 해선 안되는 말 (0) | 2021.08.14 |